作為一種基因遞送工具,腺相關(guān)病毒(AAV)在基因治療和基礎(chǔ)研究中發(fā)揮著重要作用。AAV具備宿主范圍廣泛、安全性高、免疫原性低、表達(dá)穩(wěn)定和物理性質(zhì)穩(wěn)定等優(yōu)勢,已廣泛應(yīng)用于多種細(xì)胞及動(dòng)物模型。
提供一系列高品質(zhì)的AAV產(chǎn)品。產(chǎn)品涵蓋多種血清型與報(bào)告基因,可滿足您在體外細(xì)胞感染和體內(nèi)動(dòng)物實(shí)驗(yàn)中的多樣化科研需求。
產(chǎn)品核心優(yōu)勢
1. 成熟的無血清懸浮培養(yǎng)體系
可規(guī)?;糯蟮臒o血清懸浮培養(yǎng)技術(shù),確保病毒產(chǎn)量高、批次間一致性強(qiáng)
2. 多種血清型純化平臺(tái)
覆蓋常見AAV血清型(如AAV1, 2, 5, 6, 8, 9)
3. 免疫原性低
當(dāng)AAV用局部大劑量感染肌肉、腦、眼等組織時(shí),不易造成免疫反應(yīng)
4. 宿主范圍廣
AAV可以感染分裂細(xì)胞和非分裂細(xì)胞
5. 表達(dá)穩(wěn)定
AAV滴度可至5E+13GC/mL,并可在體內(nèi)長期穩(wěn)定表達(dá)
使用指南
體外細(xì)胞感染
AAV病毒體積=最佳MOI×細(xì)胞數(shù)目/病毒滴度
例如,如果目的細(xì)胞的最佳MOI=10000,需要感染105的細(xì)胞,共計(jì)需要109 GC的病毒.如果病毒滴度為1×1012 GC/mL,那么就需要將1ul的病毒加入培養(yǎng)基中。
易感細(xì)胞MOI建議:1000-50000
難感細(xì)胞MOI 建議:2000000
強(qiáng)烈建議:使用含GFP或Luciferase的AAV進(jìn)行預(yù)實(shí)驗(yàn),確定最佳MOI。
哺乳動(dòng)物細(xì)胞轉(zhuǎn)導(dǎo)流程
轉(zhuǎn)導(dǎo)前1天
將靶細(xì)胞接種到培養(yǎng)皿中,調(diào)整細(xì)胞量使轉(zhuǎn)導(dǎo)時(shí)融合度為30%-50%。
37°C、5% CO?培養(yǎng)箱中培養(yǎng)18-20小時(shí)。
第1天
輕柔混勻病毒液,與適量培養(yǎng)基混合(建議培養(yǎng)基用量約100 μl/cm2,如6孔板每孔用1 ml)。
移除細(xì)胞原有培養(yǎng)基,加入含病毒培養(yǎng)基。
輕搖培養(yǎng)板使分布均勻,37°C、5% CO?培養(yǎng)過夜(或縮短至6-8小時(shí)以減少細(xì)胞毒性)。
第2天
移除含病毒培養(yǎng)基,更換為新鮮完全培養(yǎng)基。
繼續(xù)培養(yǎng)過夜。
第3天及之后
通常在轉(zhuǎn)導(dǎo)后24-48小時(shí),目的基因表達(dá)明顯,可進(jìn)行后續(xù)分析。
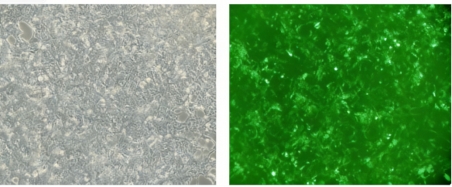
使用表達(dá)綠色熒光蛋白的AAV2型腺相關(guān)病毒以MOI=10000轉(zhuǎn)導(dǎo)293T細(xì)胞。100×參數(shù)下拍照。左圖:明視野;右圖:綠色熒光。
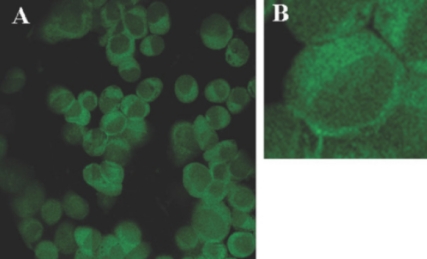
AAV/IE1在HEK293細(xì)胞中呈陽性表達(dá)。A:原始放大倍數(shù) 20×;B:原始放大倍數(shù) 63×。
體內(nèi)動(dòng)物注射(以小鼠為例)
推薦起始劑量(按體重):
為了確定用于小鼠或其他小動(dòng)物注射的AAV最佳量,建議首次測試三種劑量:1011、1012和1013 GC/kg。
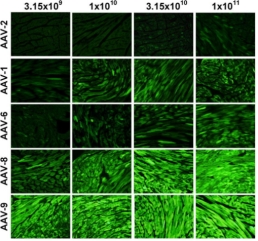
注射5種血清型(1/2/6/8/9)的AAV-eGFP載體至小鼠體內(nèi)轉(zhuǎn)染心臟
假設(shè)您的小鼠是20克,三種劑量是2x109、2x1010和2x1011 GC/小鼠。如果正在進(jìn)行非局部注射,您可能還需加入更高的劑量,如4x1011 GC/小鼠。請注意,這些是針對小鼠的通用指南,可能不適用于大型動(dòng)物模型(如豬、非人靈長類動(dòng)物)。
質(zhì)量控制體系
檢測項(xiàng)目 | 檢測方法 |
鑒別 | PCR + Sanger測序(目的基因序列驗(yàn)證) |
含量 | qPCR(基因組滴度) |
純度 | SDS-PAGE(衣殼蛋白鑒別) |
空殼率 | AUC 檢測 |
安全性 | 凝膠限度法(內(nèi)毒素檢測) |
產(chǎn)品目錄
(一)Luciferase 系列
產(chǎn)品名稱 | 貨號(hào) | 產(chǎn)品描述 |
AAV1-pAV-CMV-luciferase | FBX9501 | 報(bào)告基因 AAV |
AAV2-pAV-CMV-Luciferase | FBX9502 | 報(bào)告基因 AAV |
AAV5-pAV-CMV-Luciferase | FBX9503 | 報(bào)告基因 AAV |
AAV6-pAV-CMV-Luciferase | FBX9504 | 報(bào)告基因 AAV |
AAV8-pAV-CMV-Luciferase | FBX9505 | 報(bào)告基因 AAV |
AAV9-pAV-CMV-Luciferase | FBX9506 | 報(bào)告基因 AAV |
(二)GFP 系列
產(chǎn)品名稱 | 貨號(hào) | 產(chǎn)品描述 |
MyoAAV 1A-pAV-CMV-GFP | FBX9507 | 報(bào)告基因 AAV |
AAV2-pAV-CMV-GFP | FBX9508 | 報(bào)告基因 AAV |
AAV8-pAV-CMV-GFP | FBX9509 | 報(bào)告基因 AAV |
AAV9-pAV-CMV-GFP | FBX9510 | 報(bào)告基因 AAV |
(三)空殼 AAV
產(chǎn)品名稱 | 貨號(hào) | 產(chǎn)品描述 |
AAV2 空殼病毒 | FBX9511 | 空殼 AAV |
AAV5 空殼病毒 | FBX9512 | 空殼 AAV |
AAV6 空殼病毒 | FBX9513 | 空殼 AAV |
AAV8 空殼病毒 | FBX9514 | 空殼 AAV |
AAV9 空殼病毒 | FBX9515 | 空殼 AAV |
運(yùn)輸與保存
運(yùn)輸:全程干冰冷鏈
長期保存:-80°C(穩(wěn)定性 ≥1年)
短期保存:-20°C(≤2-3周)或 4°C(融解后,1-2周)
使用前:4°C緩慢融化
分裝建議:按單次用量分裝,避免反復(fù)凍融(雖AAV較穩(wěn)定,但仍建議最大限度保護(hù)活性)
參考文獻(xiàn)
1. Yu Y, et al.Protective CD8+ T-cell responses to cytomegalovirus driven by rAAV/GFP/IE1 loading of dendritic cells. Chiriva-Internati M -Journal of translational medicine(2008)
2. Prasad KM,et al.Robust cardiomyocyte-specific gene expression following systemic injection of AAV: in vivo gene delivery follows a Poisson distribution. French BA -Gene therapy(2010)
作為一種基因遞送工具,腺相關(guān)病毒(AAV)在基因治療和基礎(chǔ)研究中發(fā)揮著重要作用。AAV具備宿主范圍廣泛、安全性高、免疫原性低、表達(dá)穩(wěn)定和物理性質(zhì)穩(wěn)定等優(yōu)勢,已廣泛應(yīng)用于多種細(xì)胞及動(dòng)物模型。

提供一系列高品質(zhì)的AAV產(chǎn)品。產(chǎn)品涵蓋多種血清型與報(bào)告基因,可滿足您在體外細(xì)胞感染和體內(nèi)動(dòng)物實(shí)驗(yàn)中的多樣化科研需求。
產(chǎn)品核心優(yōu)勢
1. 成熟的無血清懸浮培養(yǎng)體系
可規(guī)?;糯蟮臒o血清懸浮培養(yǎng)技術(shù),確保病毒產(chǎn)量高、批次間一致性強(qiáng)
2. 多種血清型純化平臺(tái)
覆蓋常見AAV血清型(如AAV1, 2, 5, 6, 8, 9)
3. 免疫原性低
當(dāng)AAV用局部大劑量感染肌肉、腦、眼等組織時(shí),不易造成免疫反應(yīng)
4. 宿主范圍廣
AAV可以感染分裂細(xì)胞和非分裂細(xì)胞
5. 表達(dá)穩(wěn)定
AAV滴度可至5E+13GC/mL,并可在體內(nèi)長期穩(wěn)定表達(dá)
使用指南
體外細(xì)胞感染
AAV病毒體積=最佳MOI×細(xì)胞數(shù)目/病毒滴度
例如,如果目的細(xì)胞的最佳MOI=10000,需要感染105的細(xì)胞,共計(jì)需要109 GC的病毒.如果病毒滴度為1×1012 GC/mL,那么就需要將1ul的病毒加入培養(yǎng)基中。
易感細(xì)胞MOI建議:1000-50000
難感細(xì)胞MOI 建議:2000000
強(qiáng)烈建議:使用含GFP或Luciferase的AAV進(jìn)行預(yù)實(shí)驗(yàn),確定最佳MOI。
哺乳動(dòng)物細(xì)胞轉(zhuǎn)導(dǎo)流程
轉(zhuǎn)導(dǎo)前1天
將靶細(xì)胞接種到培養(yǎng)皿中,調(diào)整細(xì)胞量使轉(zhuǎn)導(dǎo)時(shí)融合度為30%-50%。
37°C、5% CO?培養(yǎng)箱中培養(yǎng)18-20小時(shí)。
第1天
輕柔混勻病毒液,與適量培養(yǎng)基混合(建議培養(yǎng)基用量約100 μl/cm2,如6孔板每孔用1 ml)。
移除細(xì)胞原有培養(yǎng)基,加入含病毒培養(yǎng)基。
輕搖培養(yǎng)板使分布均勻,37°C、5% CO?培養(yǎng)過夜(或縮短至6-8小時(shí)以減少細(xì)胞毒性)。
第2天
移除含病毒培養(yǎng)基,更換為新鮮完全培養(yǎng)基。
繼續(xù)培養(yǎng)過夜。
第3天及之后
通常在轉(zhuǎn)導(dǎo)后24-48小時(shí),目的基因表達(dá)明顯,可進(jìn)行后續(xù)分析。

使用表達(dá)綠色熒光蛋白的AAV2型腺相關(guān)病毒以MOI=10000轉(zhuǎn)導(dǎo)293T細(xì)胞。100×參數(shù)下拍照。左圖:明視野;右圖:綠色熒光。

AAV/IE1在HEK293細(xì)胞中呈陽性表達(dá)。A:原始放大倍數(shù) 20×;B:原始放大倍數(shù) 63×。
體內(nèi)動(dòng)物注射(以小鼠為例)
推薦起始劑量(按體重):
為了確定用于小鼠或其他小動(dòng)物注射的AAV最佳量,建議首次測試三種劑量:1011、1012和1013 GC/kg。

注射5種血清型(1/2/6/8/9)的AAV-eGFP載體至小鼠體內(nèi)轉(zhuǎn)染心臟
假設(shè)您的小鼠是20克,三種劑量是2x109、2x1010和2x1011 GC/小鼠。如果正在進(jìn)行非局部注射,您可能還需加入更高的劑量,如4x1011 GC/小鼠。請注意,這些是針對小鼠的通用指南,可能不適用于大型動(dòng)物模型(如豬、非人靈長類動(dòng)物)。
質(zhì)量控制體系
檢測項(xiàng)目 | 檢測方法 |
鑒別 | PCR + Sanger測序(目的基因序列驗(yàn)證) |
含量 | qPCR(基因組滴度) |
純度 | SDS-PAGE(衣殼蛋白鑒別) |
空殼率 | AUC 檢測 |
安全性 | 凝膠限度法(內(nèi)毒素檢測) |
產(chǎn)品目錄
(一)Luciferase 系列
產(chǎn)品名稱 | 貨號(hào) | 產(chǎn)品描述 |
AAV1-pAV-CMV-luciferase | FBX9501 | 報(bào)告基因 AAV |
AAV2-pAV-CMV-Luciferase | FBX9502 | 報(bào)告基因 AAV |
AAV5-pAV-CMV-Luciferase | FBX9503 | 報(bào)告基因 AAV |
AAV6-pAV-CMV-Luciferase | FBX9504 | 報(bào)告基因 AAV |
AAV8-pAV-CMV-Luciferase | FBX9505 | 報(bào)告基因 AAV |
AAV9-pAV-CMV-Luciferase | FBX9506 | 報(bào)告基因 AAV |
(二)GFP 系列
產(chǎn)品名稱 | 貨號(hào) | 產(chǎn)品描述 |
MyoAAV 1A-pAV-CMV-GFP | FBX9507 | 報(bào)告基因 AAV |
AAV2-pAV-CMV-GFP | FBX9508 | 報(bào)告基因 AAV |
AAV8-pAV-CMV-GFP | FBX9509 | 報(bào)告基因 AAV |
AAV9-pAV-CMV-GFP | FBX9510 | 報(bào)告基因 AAV |
(三)空殼 AAV
產(chǎn)品名稱 | 貨號(hào) | 產(chǎn)品描述 |
AAV2 空殼病毒 | FBX9511 | 空殼 AAV |
AAV5 空殼病毒 | FBX9512 | 空殼 AAV |
AAV6 空殼病毒 | FBX9513 | 空殼 AAV |
AAV8 空殼病毒 | FBX9514 | 空殼 AAV |
AAV9 空殼病毒 | FBX9515 | 空殼 AAV |
運(yùn)輸與保存
運(yùn)輸:全程干冰冷鏈
長期保存:-80°C(穩(wěn)定性 ≥1年)
短期保存:-20°C(≤2-3周)或 4°C(融解后,1-2周)
使用前:4°C緩慢融化
分裝建議:按單次用量分裝,避免反復(fù)凍融(雖AAV較穩(wěn)定,但仍建議最大限度保護(hù)活性)
參考文獻(xiàn)
1. Yu Y, et al.Protective CD8+ T-cell responses to cytomegalovirus driven by rAAV/GFP/IE1 loading of dendritic cells. Chiriva-Internati M -Journal of translational medicine(2008)
2. Prasad KM,et al.Robust cardiomyocyte-specific gene expression following systemic injection of AAV: in vivo gene delivery follows a Poisson distribution. French BA -Gene therapy(2010)



