摘要:研究創(chuàng)新性地利用非致病性共生菌脆弱擬桿菌來源的外膜囊泡作為遞送載體,裝載抗IL-1β單鏈可變區(qū)片段(scFv),并偶聯(lián)腎臟靶向肽(KKEEE)3K,構(gòu)建了新型納米藥物OMV-(KKEEE)3K-scFv。
慢性腎臟?。–KD)影響全球10%–15%的成年人,持續(xù)性慢性炎癥是推動其發(fā)生發(fā)展的關鍵因素。白細胞介素-1β(IL-1β)在多種實驗性和人類腎臟疾病中扮演核心角色,然而,現(xiàn)有的抗IL-1β抗體療法面臨系統(tǒng)性副作用和生產(chǎn)成本高昂等瓶頸,限制了其在CKD治療中的應用。外膜囊泡(OMV)是革蘭氏陰性菌天然分泌的脂質(zhì)雙層納米結(jié)構(gòu),具有生物分子遞送和特定組織靶向能力。本研究選用非致病性共生菌脆弱擬桿菌(Bacteroides fragilis)來源的OMV(BF-OMV)作為藥物載體,其脂多糖(LPS)內(nèi)毒素活性較低,免疫原性弱。為解決腎臟靶向難題,研究者將腎臟靶向肽(KKEEE)3K偶聯(lián)至OMV表面,并裝載更易生產(chǎn)、分子量更小的抗IL-1β單鏈可變區(qū)片段(scFv),構(gòu)建了新型納米藥物OMV-(KKEEE)3K-scFv,旨在增強藥物在腎臟的富集,提高治療效率和安全性。

圖1 脆弱擬桿菌外膜囊泡遞送單鏈抗IL-1β抗體減輕慢性腎臟病腎小管炎癥
通過基因工程技術在E. coli T7表達系統(tǒng)中成功表達并純化了分子量約為28 kDa的重組IL-1β scFv,其具有良好的中和活性和對人、鼠IL-1β的高親和力。從脆弱擬桿菌NCTC9343菌株的培養(yǎng)上清中通過超速離心法提取OMV,并通過超聲加載scFv,利用無銅點擊化學反應將(KKEEE)3K肽偶聯(lián)到OMV表面,形成OMV-(KKEEE)3K-scFv。對制備的納米顆粒進行了形貌、粒徑、電位、載藥效率、純度、無菌及內(nèi)毒素含量等多方面的質(zhì)量控制。在體外高葡萄糖(HG)誘導的小鼠原代腎小管上皮細胞(PTECs)炎癥模型以及鏈脲佐菌素(STZ)誘導的糖尿病腎?。―N)小鼠模型、MRL/lpr狼瘡性腎炎(LN)小鼠模型和單側(cè)輸尿管梗阻(UUO)小鼠模型中,系統(tǒng)評估了OMV-(KKEEE)3K-scFv的安全性、藥代動力學、生物分布及其抗炎和腎臟保護功效。
OMV-(KKEEE)3K-scFv的制備與表征
成功構(gòu)建的OMV-(KKEEE)3K-scFv納米顆粒呈現(xiàn)典型的雙層膜結(jié)構(gòu),粒徑均一,穩(wěn)定性好。不同批次制備的納米顆粒在形貌、粒徑、膜電位、載藥效率(約22.6%)和(KKEEE)3K偶聯(lián)量方面具有良好的一致性。蛋白組學分析顯示不同批次OMV的蛋白組成高度相似。螯試劑(LAL)檢測表明所有制劑的內(nèi)毒素水平均低于安全閾值。
安全性評估
體外細胞毒性實驗(CCK-8)顯示,治療劑量(8.7 × 108particles/mL)的OMV-(KKEEE)3K-scFv對PTECs的活力無影響,且未引起IL-1β、TNF-α等炎癥因子表達升高。與E. coli來源的OMV(EC-OMV)相比,BF-OMV表現(xiàn)出更低的細胞毒性和免疫刺激性。體內(nèi)長期毒性實驗(2個月)表明,健康小鼠靜脈注射OMV-(KKEEE)3K-scFv后,主要臟器(心、肝、脾、腎)病理學未見異常,血清谷草轉(zhuǎn)氨酶(AST)、谷丙轉(zhuǎn)氨酶(ALT)以及炎癥細胞因子(IL-6, TNF-α, IL-2, IL-4)水平均在正常范圍內(nèi),證明了其良好的生物相容性。
組分功效驗證
通過UUO模型驗證了各組分功能的必要性。結(jié)果顯示,單獨的OMV、scFv、OMV-(KKEEE)3K或OMV-scFv均未能顯著改善腎臟損傷和炎癥;只有完整的OMV-(KKEEE)3K-scFv系統(tǒng)才能有效降低腎小管間質(zhì)損傷評分、纖維化評分、CD68+炎癥細胞浸潤以及腎臟MCP-1、TNF-α、IL-6的表達,證實了OMV遞送、(KKEEE)3K靶向和scFv中和功能的協(xié)同作用不可或缺。
體外抗炎功效
在高葡萄糖誘導的PTECs炎癥模型中,(KKEEE)3K修飾顯著增強了OMV的細胞攝取。OMV-(KKEEE)3K-scFv處理能顯著降低HG誘導的TNF-α、IL-6、MCP-1的mRNA和蛋白表達水平,抑制NF-κB通路關鍵蛋白磷酸化p65(p-p65)的表達,并減少細胞培養(yǎng)上清中IL-1β的分泌。
體內(nèi)藥代動力學與生物分布
體外釋放實驗表明OMV-(KKEEE)3K-scFv能實現(xiàn)scFv的緩釋。在DN小鼠模型中,與游離scFv相比,OMV-(KKEEE)3K-scFv顯著延長了scFv在血液中的循環(huán)時間,并大幅提高了scFv在腎臟組織的蓄積濃度,且在注射后48小時仍能在腎臟檢測到較高水平的scFv?;铙w成像顯示OMV-(KKEEE)3K-scFv在腎臟的熒光信號顯著強于未修飾的OMV,且主要富集在病變側(cè)腎臟。免疫熒光染色證實scFv與腎小管細胞標志物megalin共定位,說明其通過megalin受體介導的內(nèi)吞作用進入腎小管細胞。
體內(nèi)治療效果
在STZ誘導的DN小鼠模型中,OMV-(KKEEE)3K-scFv治療能顯著改善腎小管形態(tài),減輕腎間質(zhì)纖維化和腎小管基底膜增厚,降低尿中性粒細胞明膠酶相關脂質(zhì)運載蛋白(NGAL)、腎損傷分子-1(Kim-1)水平和尿白蛋白/肌酐比值(ACR),但對血糖和體重無影響。同時,治療組腎臟CD68+炎癥細胞浸潤和MCP-1表達減少,TNF-α、IL-6、MCP-1的mRNA和蛋白水平下降,NF-κB通路活化被抑制,血清IL-1β、IL-6、TNF-α水平也顯著降低。
在LN和UUO小鼠模型中,OMV-(KKEEE)3K-scFv同樣表現(xiàn)出顯著的抗炎和腎臟保護作用,能夠減輕腎小管間質(zhì)炎癥細胞浸潤、纖維化程度,降低腎臟炎癥因子表達和血清炎癥指標。
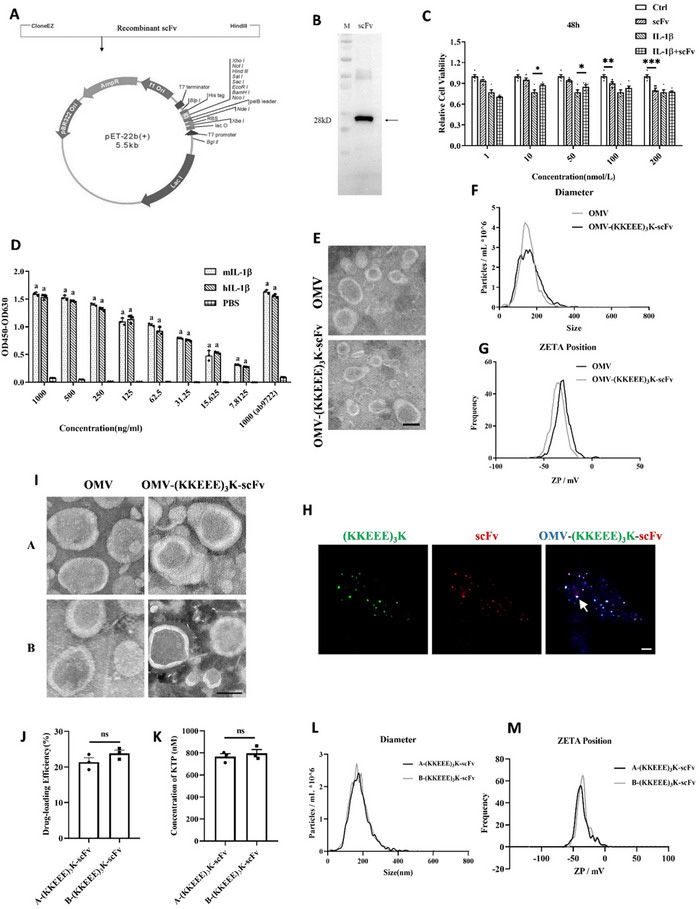
圖2 IL-1β單鏈抗體的制備及OMV-(KKEEE)3K-scFv融合蛋白的構(gòu)建
討論
本研究首次成功利用益生菌來源的OMV作為遞送載體,構(gòu)建了靶向腎臟的抗IL-1β納米藥物OMV-(KKEEE)3K-scFv。該系統(tǒng)巧妙結(jié)合了BF-OMV的低免疫原性和生物相容性、(KKEEE)3K肽的腎臟靶向能力以及scFv對IL-1β的高效中和作用,實現(xiàn)了藥物在腎臟病變部位的精準遞送和持續(xù)釋放。其在DN、LN、UUO三種不同病因的CKD模型中均能有效緩解腎小管炎癥和損傷,作用機制與抑制IL-1β/NF-κB信號通路密切相關。該研究為開發(fā)針對CKD及其他器官特異性炎癥疾病的靶向療法提供了新思路和實驗依據(jù),展示了細菌OMV作為新型藥物遞送平臺的巨大應用潛力。未來研究可進一步優(yōu)化OMV的尺寸和表面修飾,以減少非靶器官積累,并探索長期給藥的免疫應答問題。
參考資料
[1] Single-Chain Anti-IL-1β Antibody Carried by Outer Membrane Vesicles of Bacteroides fragilis Alleviates Tubular Inflammation in Chronic Kidney Disease
摘要:研究創(chuàng)新性地利用非致病性共生菌脆弱擬桿菌來源的外膜囊泡作為遞送載體,裝載抗IL-1β單鏈可變區(qū)片段(scFv),并偶聯(lián)腎臟靶向肽(KKEEE)3K,構(gòu)建了新型納米藥物OMV-(KKEEE)3K-scFv。
慢性腎臟?。–KD)影響全球10%–15%的成年人,持續(xù)性慢性炎癥是推動其發(fā)生發(fā)展的關鍵因素。白細胞介素-1β(IL-1β)在多種實驗性和人類腎臟疾病中扮演核心角色,然而,現(xiàn)有的抗IL-1β抗體療法面臨系統(tǒng)性副作用和生產(chǎn)成本高昂等瓶頸,限制了其在CKD治療中的應用。外膜囊泡(OMV)是革蘭氏陰性菌天然分泌的脂質(zhì)雙層納米結(jié)構(gòu),具有生物分子遞送和特定組織靶向能力。本研究選用非致病性共生菌脆弱擬桿菌(Bacteroides fragilis)來源的OMV(BF-OMV)作為藥物載體,其脂多糖(LPS)內(nèi)毒素活性較低,免疫原性弱。為解決腎臟靶向難題,研究者將腎臟靶向肽(KKEEE)3K偶聯(lián)至OMV表面,并裝載更易生產(chǎn)、分子量更小的抗IL-1β單鏈可變區(qū)片段(scFv),構(gòu)建了新型納米藥物OMV-(KKEEE)3K-scFv,旨在增強藥物在腎臟的富集,提高治療效率和安全性。

圖1 脆弱擬桿菌外膜囊泡遞送單鏈抗IL-1β抗體減輕慢性腎臟病腎小管炎癥
通過基因工程技術在E. coli T7表達系統(tǒng)中成功表達并純化了分子量約為28 kDa的重組IL-1β scFv,其具有良好的中和活性和對人、鼠IL-1β的高親和力。從脆弱擬桿菌NCTC9343菌株的培養(yǎng)上清中通過超速離心法提取OMV,并通過超聲加載scFv,利用無銅點擊化學反應將(KKEEE)3K肽偶聯(lián)到OMV表面,形成OMV-(KKEEE)3K-scFv。對制備的納米顆粒進行了形貌、粒徑、電位、載藥效率、純度、無菌及內(nèi)毒素含量等多方面的質(zhì)量控制。在體外高葡萄糖(HG)誘導的小鼠原代腎小管上皮細胞(PTECs)炎癥模型以及鏈脲佐菌素(STZ)誘導的糖尿病腎?。―N)小鼠模型、MRL/lpr狼瘡性腎炎(LN)小鼠模型和單側(cè)輸尿管梗阻(UUO)小鼠模型中,系統(tǒng)評估了OMV-(KKEEE)3K-scFv的安全性、藥代動力學、生物分布及其抗炎和腎臟保護功效。
OMV-(KKEEE)3K-scFv的制備與表征
成功構(gòu)建的OMV-(KKEEE)3K-scFv納米顆粒呈現(xiàn)典型的雙層膜結(jié)構(gòu),粒徑均一,穩(wěn)定性好。不同批次制備的納米顆粒在形貌、粒徑、膜電位、載藥效率(約22.6%)和(KKEEE)3K偶聯(lián)量方面具有良好的一致性。蛋白組學分析顯示不同批次OMV的蛋白組成高度相似。螯試劑(LAL)檢測表明所有制劑的內(nèi)毒素水平均低于安全閾值。
安全性評估
體外細胞毒性實驗(CCK-8)顯示,治療劑量(8.7 × 108particles/mL)的OMV-(KKEEE)3K-scFv對PTECs的活力無影響,且未引起IL-1β、TNF-α等炎癥因子表達升高。與E. coli來源的OMV(EC-OMV)相比,BF-OMV表現(xiàn)出更低的細胞毒性和免疫刺激性。體內(nèi)長期毒性實驗(2個月)表明,健康小鼠靜脈注射OMV-(KKEEE)3K-scFv后,主要臟器(心、肝、脾、腎)病理學未見異常,血清谷草轉(zhuǎn)氨酶(AST)、谷丙轉(zhuǎn)氨酶(ALT)以及炎癥細胞因子(IL-6, TNF-α, IL-2, IL-4)水平均在正常范圍內(nèi),證明了其良好的生物相容性。
組分功效驗證
通過UUO模型驗證了各組分功能的必要性。結(jié)果顯示,單獨的OMV、scFv、OMV-(KKEEE)3K或OMV-scFv均未能顯著改善腎臟損傷和炎癥;只有完整的OMV-(KKEEE)3K-scFv系統(tǒng)才能有效降低腎小管間質(zhì)損傷評分、纖維化評分、CD68+炎癥細胞浸潤以及腎臟MCP-1、TNF-α、IL-6的表達,證實了OMV遞送、(KKEEE)3K靶向和scFv中和功能的協(xié)同作用不可或缺。
體外抗炎功效
在高葡萄糖誘導的PTECs炎癥模型中,(KKEEE)3K修飾顯著增強了OMV的細胞攝取。OMV-(KKEEE)3K-scFv處理能顯著降低HG誘導的TNF-α、IL-6、MCP-1的mRNA和蛋白表達水平,抑制NF-κB通路關鍵蛋白磷酸化p65(p-p65)的表達,并減少細胞培養(yǎng)上清中IL-1β的分泌。
體內(nèi)藥代動力學與生物分布
體外釋放實驗表明OMV-(KKEEE)3K-scFv能實現(xiàn)scFv的緩釋。在DN小鼠模型中,與游離scFv相比,OMV-(KKEEE)3K-scFv顯著延長了scFv在血液中的循環(huán)時間,并大幅提高了scFv在腎臟組織的蓄積濃度,且在注射后48小時仍能在腎臟檢測到較高水平的scFv?;铙w成像顯示OMV-(KKEEE)3K-scFv在腎臟的熒光信號顯著強于未修飾的OMV,且主要富集在病變側(cè)腎臟。免疫熒光染色證實scFv與腎小管細胞標志物megalin共定位,說明其通過megalin受體介導的內(nèi)吞作用進入腎小管細胞。
體內(nèi)治療效果
在STZ誘導的DN小鼠模型中,OMV-(KKEEE)3K-scFv治療能顯著改善腎小管形態(tài),減輕腎間質(zhì)纖維化和腎小管基底膜增厚,降低尿中性粒細胞明膠酶相關脂質(zhì)運載蛋白(NGAL)、腎損傷分子-1(Kim-1)水平和尿白蛋白/肌酐比值(ACR),但對血糖和體重無影響。同時,治療組腎臟CD68+炎癥細胞浸潤和MCP-1表達減少,TNF-α、IL-6、MCP-1的mRNA和蛋白水平下降,NF-κB通路活化被抑制,血清IL-1β、IL-6、TNF-α水平也顯著降低。
在LN和UUO小鼠模型中,OMV-(KKEEE)3K-scFv同樣表現(xiàn)出顯著的抗炎和腎臟保護作用,能夠減輕腎小管間質(zhì)炎癥細胞浸潤、纖維化程度,降低腎臟炎癥因子表達和血清炎癥指標。

圖2 IL-1β單鏈抗體的制備及OMV-(KKEEE)3K-scFv融合蛋白的構(gòu)建
討論
本研究首次成功利用益生菌來源的OMV作為遞送載體,構(gòu)建了靶向腎臟的抗IL-1β納米藥物OMV-(KKEEE)3K-scFv。該系統(tǒng)巧妙結(jié)合了BF-OMV的低免疫原性和生物相容性、(KKEEE)3K肽的腎臟靶向能力以及scFv對IL-1β的高效中和作用,實現(xiàn)了藥物在腎臟病變部位的精準遞送和持續(xù)釋放。其在DN、LN、UUO三種不同病因的CKD模型中均能有效緩解腎小管炎癥和損傷,作用機制與抑制IL-1β/NF-κB信號通路密切相關。該研究為開發(fā)針對CKD及其他器官特異性炎癥疾病的靶向療法提供了新思路和實驗依據(jù),展示了細菌OMV作為新型藥物遞送平臺的巨大應用潛力。未來研究可進一步優(yōu)化OMV的尺寸和表面修飾,以減少非靶器官積累,并探索長期給藥的免疫應答問題。
參考資料
[1] Single-Chain Anti-IL-1β Antibody Carried by Outer Membrane Vesicles of Bacteroides fragilis Alleviates Tubular Inflammation in Chronic Kidney Disease



