研究人員已經(jīng)確定了癌癥進化中一個以前未被認識到的關鍵角色:發(fā)生在基因組特定區(qū)域的突變簇。這些突變簇有助于約10%的人類癌癥的進展,并可用于預測患者的生存率。
該研究結果發(fā)表在2月9日出版的《Nature》雜志上。
這項研究揭示了一類被稱為聚集體細胞突變的突變——聚集意味著它們在細胞基因組的特定區(qū)域聚集在一起,而體細胞意味著它們不是遺傳的,而是由內(nèi)部和外部因素引起的,比如衰老或暴露在紫外線輻射下。
到目前為止,聚集的體細胞突變一直是癌癥發(fā)展中一個有待研究的領域。但加州大學圣地亞哥分校生物工程、細胞和分子醫(yī)學教授Ludmil Alexandrov實驗室的研究人員發(fā)現(xiàn),這些突變非常不尋常,值得進一步研究。
“我們通常會看到基因組中隨機發(fā)生的體細胞突變。但當我們仔細觀察這些突變時,我們發(fā)現(xiàn)它們發(fā)生在這些熱點地區(qū)。這就像在地上扔球,然后突然看到它們聚集在一個空間,”Alexandrov說。“所以我們不禁想知道:這里發(fā)生了什么?為什么會有熱點?它們與臨床相關嗎?它們能告訴我們癌癥是如何發(fā)展的嗎?”
Alexandrov實驗室的生物工程博士生、該研究的第一作者Erik Bergstrom說:“聚集性突變在很大程度上被忽視了,因為它們只占所有突變的很小一部分。但通過深入研究,我們發(fā)現(xiàn)它們在人類癌癥的病因?qū)W中發(fā)揮著重要作用?!?/div>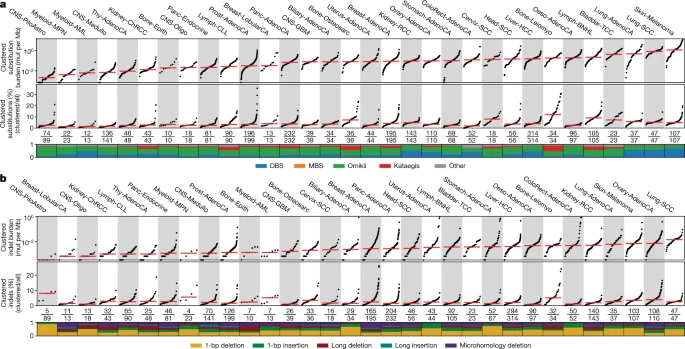
聚集體細胞突變

聚集體細胞突變
該團隊的發(fā)現(xiàn)是通過創(chuàng)建全面和詳細的已知聚集體細胞突變的地圖而實現(xiàn)的。他們首先繪制了2500多名癌癥患者基因組中的所有突變(聚集突變和非聚集突變),這項工作總共包含了30種不同的癌癥類型。研究人員使用亞歷山德羅夫?qū)嶒炇议_發(fā)的下一代人工智能方法繪制了他們的地圖。該團隊使用這些算法來檢測個體患者中的聚集突變,并闡明導致這些事件的潛在突變過程。他們發(fā)現(xiàn),在大約10%的人類癌癥中,聚集的體細胞突變有助于癌癥的進化。
更進一步,研究人員還發(fā)現(xiàn),一些癌癥驅(qū)動簇——特別是那些在已知的癌癥驅(qū)動基因中發(fā)現(xiàn)的——可以用來預測患者的總體生存率。例如,BRAF基因(黑色素瘤中廣泛觀察的驅(qū)動基因)的聚集突變的存在,比非聚集突變的個體帶來更好的總體患者生存。同時,EGFR基因(肺癌中廣泛觀察的驅(qū)動基因)的聚集突變的存在導致患者生存期的下降。
“重要的是,我們看到僅從這些基因中檢測到的聚集突變就能產(chǎn)生不同的生存率,這是可以用臨床常用的現(xiàn)有平臺檢測到的。因此,這是一個非常簡單和精確的患者生存生物標記。”
“這項出色的工作強調(diào)了開發(fā)人工智能方法來闡明腫瘤生物學的重要性,以及使用可直接轉(zhuǎn)化為臨床視線的標準平臺來發(fā)現(xiàn)和快速開發(fā)生物標志物的重要性?!蹦査拱┌Y中心主任、加州大學圣地亞哥分校癌癥研究和護理副校長Scott Lippman說?!斑@凸顯了加州大學圣地亞哥分校在結合工程方法和人工智能解決當前癌癥醫(yī)學問題方面的優(yōu)勢?!?/div>
癌癥進化的新模式
在這項研究中,研究人員還確定了導致聚集性體細胞突變的各種因素。這些因素包括紫外線輻射、飲酒、吸煙,值得注意的是,一種叫做APOBEC3的抗病毒酶的活性。
APOBEC3酶通常存在于細胞內(nèi)部,作為細胞內(nèi)部免疫反應的一部分。它們的主要工作是切斷任何進入細胞的病毒。但在癌細胞中,研究人員認為APOBEC3酶可能弊大于利。
研究人員發(fā)現(xiàn),癌細胞中通常充滿了攜帶著已知癌癥驅(qū)動基因的染色體外DNA (ecDNA)環(huán)狀結構,在單個ecDNA分子中存在著聚集的突變。研究人員將這些突變歸因于APOBEC3酶的活性。他們假設APOBEC3酶誤將外鏈DNA的環(huán)當成外來病毒,并試圖限制和切斷它們。在此過程中,APOBEC3酶導致單個ecDNA分子內(nèi)形成突變簇。這反過來又在加速癌癥進化和可能導致耐藥性方面發(fā)揮了關鍵作用。研究人員將這些聚集的突變環(huán)命名為kyklonas,這是希臘語中氣旋的意思。
Alexandrov說:“這是一種全新的腫瘤發(fā)生模式?!彼忉屨f,隨著團隊的其他發(fā)現(xiàn),“這為新的治療方法奠定了基礎,臨床醫(yī)生可以考慮限制APOBEC3酶的活性和/或針對染色體外DNA的癌癥治療?!?/div>
參考資料:
研究人員已經(jīng)確定了癌癥進化中一個以前未被認識到的關鍵角色:發(fā)生在基因組特定區(qū)域的突變簇。這些突變簇有助于約10%的人類癌癥的進展,并可用于預測患者的生存率。
該研究結果發(fā)表在2月9日出版的《Nature》雜志上。
這項研究揭示了一類被稱為聚集體細胞突變的突變——聚集意味著它們在細胞基因組的特定區(qū)域聚集在一起,而體細胞意味著它們不是遺傳的,而是由內(nèi)部和外部因素引起的,比如衰老或暴露在紫外線輻射下。
到目前為止,聚集的體細胞突變一直是癌癥發(fā)展中一個有待研究的領域。但加州大學圣地亞哥分校生物工程、細胞和分子醫(yī)學教授Ludmil Alexandrov實驗室的研究人員發(fā)現(xiàn),這些突變非常不尋常,值得進一步研究。
“我們通常會看到基因組中隨機發(fā)生的體細胞突變。但當我們仔細觀察這些突變時,我們發(fā)現(xiàn)它們發(fā)生在這些熱點地區(qū)。這就像在地上扔球,然后突然看到它們聚集在一個空間,”Alexandrov說?!八晕覀儾唤胫?這里發(fā)生了什么?為什么會有熱點?它們與臨床相關嗎?它們能告訴我們癌癥是如何發(fā)展的嗎?”
Alexandrov實驗室的生物工程博士生、該研究的第一作者Erik Bergstrom說:“聚集性突變在很大程度上被忽視了,因為它們只占所有突變的很小一部分。但通過深入研究,我們發(fā)現(xiàn)它們在人類癌癥的病因?qū)W中發(fā)揮著重要作用?!?/div>
聚集體細胞突變

聚集體細胞突變
該團隊的發(fā)現(xiàn)是通過創(chuàng)建全面和詳細的已知聚集體細胞突變的地圖而實現(xiàn)的。他們首先繪制了2500多名癌癥患者基因組中的所有突變(聚集突變和非聚集突變),這項工作總共包含了30種不同的癌癥類型。研究人員使用亞歷山德羅夫?qū)嶒炇议_發(fā)的下一代人工智能方法繪制了他們的地圖。該團隊使用這些算法來檢測個體患者中的聚集突變,并闡明導致這些事件的潛在突變過程。他們發(fā)現(xiàn),在大約10%的人類癌癥中,聚集的體細胞突變有助于癌癥的進化。
更進一步,研究人員還發(fā)現(xiàn),一些癌癥驅(qū)動簇——特別是那些在已知的癌癥驅(qū)動基因中發(fā)現(xiàn)的——可以用來預測患者的總體生存率。例如,BRAF基因(黑色素瘤中廣泛觀察的驅(qū)動基因)的聚集突變的存在,比非聚集突變的個體帶來更好的總體患者生存。同時,EGFR基因(肺癌中廣泛觀察的驅(qū)動基因)的聚集突變的存在導致患者生存期的下降。
“重要的是,我們看到僅從這些基因中檢測到的聚集突變就能產(chǎn)生不同的生存率,這是可以用臨床常用的現(xiàn)有平臺檢測到的。因此,這是一個非常簡單和精確的患者生存生物標記。”
“這項出色的工作強調(diào)了開發(fā)人工智能方法來闡明腫瘤生物學的重要性,以及使用可直接轉(zhuǎn)化為臨床視線的標準平臺來發(fā)現(xiàn)和快速開發(fā)生物標志物的重要性?!蹦査拱┌Y中心主任、加州大學圣地亞哥分校癌癥研究和護理副校長Scott Lippman說?!斑@凸顯了加州大學圣地亞哥分校在結合工程方法和人工智能解決當前癌癥醫(yī)學問題方面的優(yōu)勢?!?/div>
癌癥進化的新模式
在這項研究中,研究人員還確定了導致聚集性體細胞突變的各種因素。這些因素包括紫外線輻射、飲酒、吸煙,值得注意的是,一種叫做APOBEC3的抗病毒酶的活性。
APOBEC3酶通常存在于細胞內(nèi)部,作為細胞內(nèi)部免疫反應的一部分。它們的主要工作是切斷任何進入細胞的病毒。但在癌細胞中,研究人員認為APOBEC3酶可能弊大于利。
研究人員發(fā)現(xiàn),癌細胞中通常充滿了攜帶著已知癌癥驅(qū)動基因的染色體外DNA (ecDNA)環(huán)狀結構,在單個ecDNA分子中存在著聚集的突變。研究人員將這些突變歸因于APOBEC3酶的活性。他們假設APOBEC3酶誤將外鏈DNA的環(huán)當成外來病毒,并試圖限制和切斷它們。在此過程中,APOBEC3酶導致單個ecDNA分子內(nèi)形成突變簇。這反過來又在加速癌癥進化和可能導致耐藥性方面發(fā)揮了關鍵作用。研究人員將這些聚集的突變環(huán)命名為kyklonas,這是希臘語中氣旋的意思。
Alexandrov說:“這是一種全新的腫瘤發(fā)生模式。”他解釋說,隨著團隊的其他發(fā)現(xiàn),“這為新的治療方法奠定了基礎,臨床醫(yī)生可以考慮限制APOBEC3酶的活性和/或針對染色體外DNA的癌癥治療。”
參考資料:



