摘要:系統(tǒng)闡述了視網(wǎng)膜退化蛋白3(RD3)在神經(jīng)母細胞瘤(NB)惡性演進中的核心調(diào)控作用。
本研究采用14株高危神經(jīng)母細胞瘤(NB)細胞系,包括診斷期(Dx)和進展期(PD)來源的細胞,并構(gòu)建了RD3穩(wěn)定敲除(RD3-/-)和恢復(fù)(RD3+/+)的基因工程細胞模型。通過免疫印跡、免疫熒光、流式細胞術(shù)、酶聯(lián)免疫吸附試驗(ELISA)、染色質(zhì)免疫共沉淀(ChIP)、免疫共沉淀(Co-IP)等多種分子生物學(xué)技術(shù),系統(tǒng)評估了RD3對NB細胞譜系可塑性、干細胞特性、腫瘤遷移侵襲、免疫分子表達及體內(nèi)外腫瘤生長的影響。

圖1 細胞身份危機:RD3缺失在進展性神經(jīng)母細胞瘤中助長可塑性并引發(fā)免疫靜默
臨床治療壓力導(dǎo)致NB細胞獲得性RD3表達缺失。與診斷期RD3表達陽性(Dx-RD3+/+)的細胞相比,進展期RD3缺失(PD-RD3-/-)的細胞表現(xiàn)出顯著的上皮-間質(zhì)轉(zhuǎn)化(EMT)特征,包括Vimentin、N-Cadherin、Slug表達上調(diào)和E-Cadherin表達下調(diào)。同時,RD3缺失增強了細胞的遷移、侵襲能力和克隆形成能力。更重要的是,RD3缺失富集了癌癥干細胞(CSC)群體,表現(xiàn)為ALDH+細胞比例升高以及CD133、CD114、CD117等干細胞標志物陽性細胞,尤其是三陽性(CD133+CD114+CD117+)CSC群體的擴增。
在體內(nèi)實驗中,與RD3表達陽性的原發(fā)腫瘤相比,RD3缺失的轉(zhuǎn)移瘤中多能性核心轉(zhuǎn)錄因子SOX2、OCT3/4、NANOG的轉(zhuǎn)錄和翻譯水平均顯著升高。RD3缺失的轉(zhuǎn)移性病灶衍生侵襲性細胞(MSDAC)中,SOX2或NANOG的單獨敲低會導(dǎo)致其他核心多能性因子(OCT3/4、NANOG/SOX2)的表達下降,表明RD3缺失激活了一個自我強化的多能性調(diào)控回路。
通過RD3基因工程操作(敲除或恢復(fù))模型證實,RD3是NB細胞身份的關(guān)鍵決定因子。RD3缺失誘導(dǎo)了顯著的超微結(jié)構(gòu)改變,包括線粒體數(shù)量增多、脂滴積聚以及自噬體形成,提示代謝重編程。RD3缺失直接導(dǎo)致多能性核心 circuitry(SOX2、OCT3/4、NANOG)的激活,RD3蛋白可與這些轉(zhuǎn)錄因子結(jié)合,并調(diào)控其啟動子活性。功能上,RD3缺失增強了細胞的腫瘤球形成能力、BrdU摻入所代表的增殖活性以及轉(zhuǎn)移相關(guān)分子(如MMP9、ICAM1、RON-β)的表達。
RD3通過調(diào)控腫瘤細胞的免疫原性深刻影響腫瘤免疫微環(huán)境(TIME)。RD3缺失導(dǎo)致主要組織相容性復(fù)合體I類(MHC I)分子(HLA A/B、β2M)表達下調(diào),削弱了抗原呈遞能力。同時,免疫檢查點分子PDL1和CD276的表達顯著上調(diào)。機制上,RD3缺失通過激活NFκB信號通路促進PDL1轉(zhuǎn)錄。此外,RD3缺失的腫瘤細胞高表達“別吃我”信號CD24和腫瘤相關(guān)抗原GD2,但CD171表達變化不顯著。在體外共培養(yǎng)體系中,與RD3表達陽性的腫瘤細胞共培養(yǎng)的T細胞(Tc)能產(chǎn)生更多的效應(yīng)細胞因子(TNFα、IFNγ),表達更高的活化標志物(CD107a、CD137),并展現(xiàn)出更強的腫瘤細胞殺傷能力(Caspase-3活性升高);而RD3缺失則削弱了T細胞的這些效應(yīng)功能。
體內(nèi)研究進一步證實了RD3對腫瘤免疫景觀的塑造作用。與RD3表達腫瘤相比,RD3缺失腫瘤中免疫細胞浸潤模式發(fā)生改變,表現(xiàn)為CD4+和CD8+T細胞浸潤減少,T細胞活化標志物(CD44、GITR)表達降低。同時,RD3缺失腫瘤中腺苷能免疫抑制通路(CD39、CD73、A2AR)相關(guān)分子表達上調(diào),而免疫激活相關(guān)分子(如CD86、STING)表達下降。RD3恢復(fù)則能逆轉(zhuǎn)這種免疫抑制狀態(tài),促進抗腫瘤免疫。
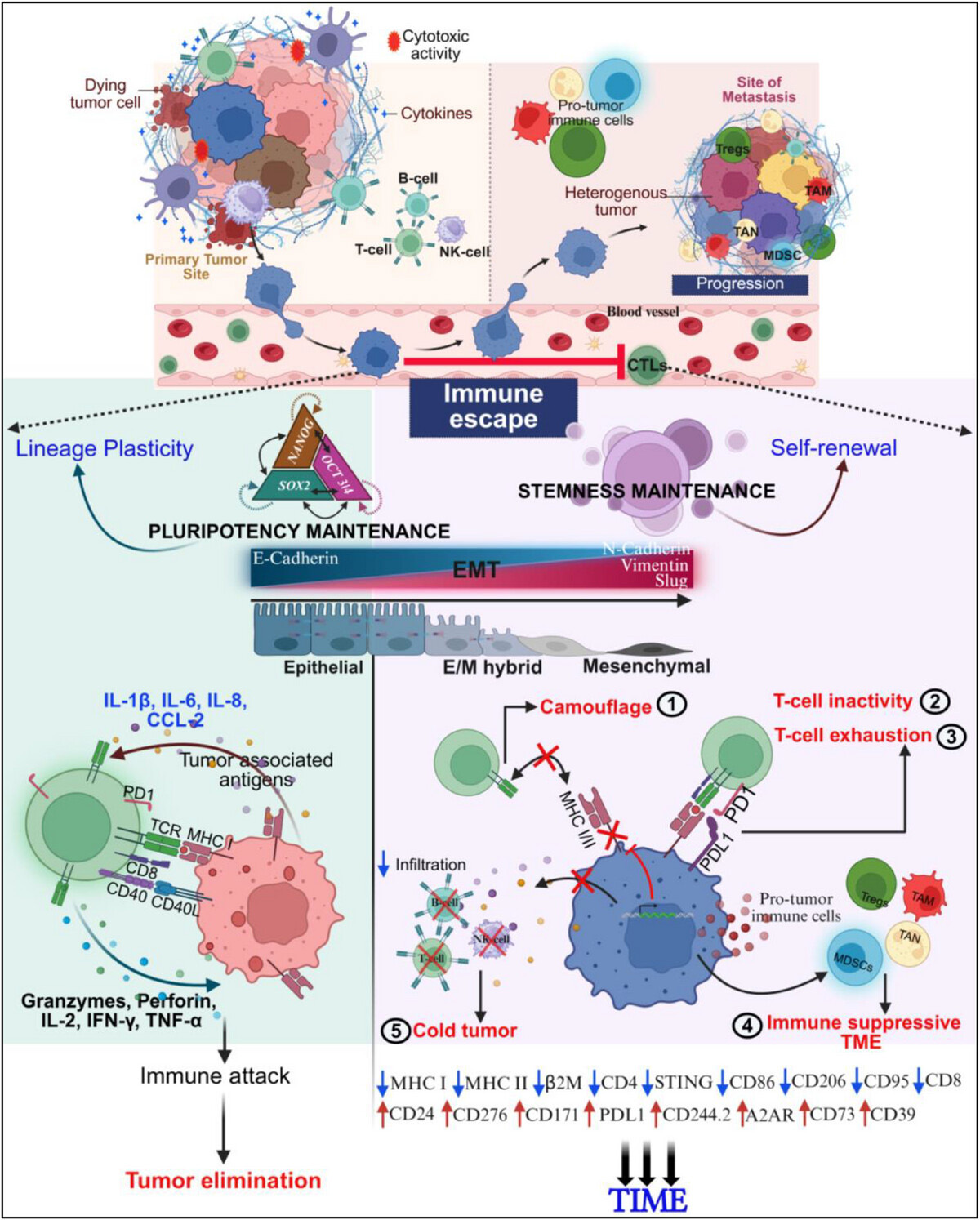
圖2 示意圖展示細胞可塑性在神經(jīng)母細胞瘤免疫逃逸中的作用
本研究確立了RD3作為神經(jīng)母細胞瘤中連接細胞可塑性與腫瘤免疫微環(huán)境重塑的核心樞紐。治療壓力誘導(dǎo)的RD3缺失,驅(qū)動腫瘤細胞發(fā)生上皮-間質(zhì)轉(zhuǎn)化(EMT)并獲得干細胞樣特性,同時通過下調(diào)抗原呈遞、上調(diào)免疫檢查點分子和激活腺苷能免疫抑制通路,協(xié)同塑造了一個免疫豁免的“冷腫瘤”微環(huán)境。RD3通過直接結(jié)合并抑制多能性轉(zhuǎn)錄因子SOX2、OCT3/4、NANOG的活性,從而約束細胞的譜系可塑性。研究結(jié)果揭示了RD3在腫瘤免疫編輯中的關(guān)鍵作用,將其定位為一個潛在的治療靶點,針對RD3通路的干預(yù)策略有望逆轉(zhuǎn)高危神經(jīng)母細胞瘤的免疫治療耐藥性。
參考資料
[1] Cellular Identity Crisis: RD3 Loss Fuels Plasticity and Immune Silence in Progressive Neuroblastoma
摘要:系統(tǒng)闡述了視網(wǎng)膜退化蛋白3(RD3)在神經(jīng)母細胞瘤(NB)惡性演進中的核心調(diào)控作用。
本研究采用14株高危神經(jīng)母細胞瘤(NB)細胞系,包括診斷期(Dx)和進展期(PD)來源的細胞,并構(gòu)建了RD3穩(wěn)定敲除(RD3-/-)和恢復(fù)(RD3+/+)的基因工程細胞模型。通過免疫印跡、免疫熒光、流式細胞術(shù)、酶聯(lián)免疫吸附試驗(ELISA)、染色質(zhì)免疫共沉淀(ChIP)、免疫共沉淀(Co-IP)等多種分子生物學(xué)技術(shù),系統(tǒng)評估了RD3對NB細胞譜系可塑性、干細胞特性、腫瘤遷移侵襲、免疫分子表達及體內(nèi)外腫瘤生長的影響。

圖1 細胞身份危機:RD3缺失在進展性神經(jīng)母細胞瘤中助長可塑性并引發(fā)免疫靜默
臨床治療壓力導(dǎo)致NB細胞獲得性RD3表達缺失。與診斷期RD3表達陽性(Dx-RD3+/+)的細胞相比,進展期RD3缺失(PD-RD3-/-)的細胞表現(xiàn)出顯著的上皮-間質(zhì)轉(zhuǎn)化(EMT)特征,包括Vimentin、N-Cadherin、Slug表達上調(diào)和E-Cadherin表達下調(diào)。同時,RD3缺失增強了細胞的遷移、侵襲能力和克隆形成能力。更重要的是,RD3缺失富集了癌癥干細胞(CSC)群體,表現(xiàn)為ALDH+細胞比例升高以及CD133、CD114、CD117等干細胞標志物陽性細胞,尤其是三陽性(CD133+CD114+CD117+)CSC群體的擴增。
在體內(nèi)實驗中,與RD3表達陽性的原發(fā)腫瘤相比,RD3缺失的轉(zhuǎn)移瘤中多能性核心轉(zhuǎn)錄因子SOX2、OCT3/4、NANOG的轉(zhuǎn)錄和翻譯水平均顯著升高。RD3缺失的轉(zhuǎn)移性病灶衍生侵襲性細胞(MSDAC)中,SOX2或NANOG的單獨敲低會導(dǎo)致其他核心多能性因子(OCT3/4、NANOG/SOX2)的表達下降,表明RD3缺失激活了一個自我強化的多能性調(diào)控回路。
通過RD3基因工程操作(敲除或恢復(fù))模型證實,RD3是NB細胞身份的關(guān)鍵決定因子。RD3缺失誘導(dǎo)了顯著的超微結(jié)構(gòu)改變,包括線粒體數(shù)量增多、脂滴積聚以及自噬體形成,提示代謝重編程。RD3缺失直接導(dǎo)致多能性核心 circuitry(SOX2、OCT3/4、NANOG)的激活,RD3蛋白可與這些轉(zhuǎn)錄因子結(jié)合,并調(diào)控其啟動子活性。功能上,RD3缺失增強了細胞的腫瘤球形成能力、BrdU摻入所代表的增殖活性以及轉(zhuǎn)移相關(guān)分子(如MMP9、ICAM1、RON-β)的表達。
RD3通過調(diào)控腫瘤細胞的免疫原性深刻影響腫瘤免疫微環(huán)境(TIME)。RD3缺失導(dǎo)致主要組織相容性復(fù)合體I類(MHC I)分子(HLA A/B、β2M)表達下調(diào),削弱了抗原呈遞能力。同時,免疫檢查點分子PDL1和CD276的表達顯著上調(diào)。機制上,RD3缺失通過激活NFκB信號通路促進PDL1轉(zhuǎn)錄。此外,RD3缺失的腫瘤細胞高表達“別吃我”信號CD24和腫瘤相關(guān)抗原GD2,但CD171表達變化不顯著。在體外共培養(yǎng)體系中,與RD3表達陽性的腫瘤細胞共培養(yǎng)的T細胞(Tc)能產(chǎn)生更多的效應(yīng)細胞因子(TNFα、IFNγ),表達更高的活化標志物(CD107a、CD137),并展現(xiàn)出更強的腫瘤細胞殺傷能力(Caspase-3活性升高);而RD3缺失則削弱了T細胞的這些效應(yīng)功能。
體內(nèi)研究進一步證實了RD3對腫瘤免疫景觀的塑造作用。與RD3表達腫瘤相比,RD3缺失腫瘤中免疫細胞浸潤模式發(fā)生改變,表現(xiàn)為CD4+和CD8+T細胞浸潤減少,T細胞活化標志物(CD44、GITR)表達降低。同時,RD3缺失腫瘤中腺苷能免疫抑制通路(CD39、CD73、A2AR)相關(guān)分子表達上調(diào),而免疫激活相關(guān)分子(如CD86、STING)表達下降。RD3恢復(fù)則能逆轉(zhuǎn)這種免疫抑制狀態(tài),促進抗腫瘤免疫。

圖2 示意圖展示細胞可塑性在神經(jīng)母細胞瘤免疫逃逸中的作用
本研究確立了RD3作為神經(jīng)母細胞瘤中連接細胞可塑性與腫瘤免疫微環(huán)境重塑的核心樞紐。治療壓力誘導(dǎo)的RD3缺失,驅(qū)動腫瘤細胞發(fā)生上皮-間質(zhì)轉(zhuǎn)化(EMT)并獲得干細胞樣特性,同時通過下調(diào)抗原呈遞、上調(diào)免疫檢查點分子和激活腺苷能免疫抑制通路,協(xié)同塑造了一個免疫豁免的“冷腫瘤”微環(huán)境。RD3通過直接結(jié)合并抑制多能性轉(zhuǎn)錄因子SOX2、OCT3/4、NANOG的活性,從而約束細胞的譜系可塑性。研究結(jié)果揭示了RD3在腫瘤免疫編輯中的關(guān)鍵作用,將其定位為一個潛在的治療靶點,針對RD3通路的干預(yù)策略有望逆轉(zhuǎn)高危神經(jīng)母細胞瘤的免疫治療耐藥性。
參考資料
[1] Cellular Identity Crisis: RD3 Loss Fuels Plasticity and Immune Silence in Progressive Neuroblastoma



