摘要:研究人員近日發(fā)現(xiàn),癌細(xì)胞中最強大的遺傳“開關(guān)”——超級增強子,會驅(qū)動異常高的基因活性。
耶路撒冷希伯來大學(xué)的研究人員近日發(fā)現(xiàn),癌細(xì)胞中最強大的遺傳“開關(guān)”——超級增強子,會驅(qū)動異常高的基因活性。這種高速運轉(zhuǎn)會給DNA帶來壓力,并可能導(dǎo)致危險的雙鏈斷裂。
癌細(xì)胞通常能夠修復(fù)這些損傷,但修復(fù)過程常常會出錯,反復(fù)的斷裂和修復(fù)會使這些區(qū)域更容易隨時間而積累突變。
簡單地說,幫助癌癥快速生長的機制也可能使DNA變得更加脆弱,這有助于解釋腫瘤如何持續(xù)演化,并在某些情況下變得更具侵襲性。
這項研究成果于1月21日發(fā)表在《Science Advances》雜志上。

圖1 超級增強子塑造癌癥中轉(zhuǎn)錄相關(guān)DNA斷裂的分布格局與修復(fù)動態(tài)
癌癥的特征是不受控制的增殖,并伴隨著致癌基因過度轉(zhuǎn)錄,這會引發(fā)轉(zhuǎn)錄應(yīng)激。這種應(yīng)激是導(dǎo)致DNA雙鏈斷裂的主要原因,進(jìn)而危及基因組穩(wěn)定性。
盡管轉(zhuǎn)錄應(yīng)激至關(guān)重要,但其整體景觀及后果仍未被充分探索。
研究人員將重點放在超級增強子上,這些片段能夠增強附近基因的活性,使驅(qū)動癌癥的基因程序保持高水平運行。
他們利用一種稱為sBLISS的基因組作圖方法,繪制出了雙鏈斷裂的詳細(xì)圖譜。雙鏈斷裂(DSB)是最嚴(yán)重的DNA損傷類型之一,其特征是DNA分子的兩條鏈同時斷裂。
這些斷裂并非隨機分布:它們聚集在由超級增強子驅(qū)動的基因內(nèi),這表明當(dāng)癌癥迫使某些基因持續(xù)表達(dá)時,可能會使系統(tǒng)承受過大的壓力,從而引發(fā)斷裂。
研究人員還追蹤了細(xì)胞用來標(biāo)記DNA損傷并調(diào)動修復(fù)機制的天然“警報”信號。他們發(fā)現(xiàn),這些高活性區(qū)域會反復(fù)發(fā)生DNA斷裂和修復(fù)。盡管這有助于腫瘤存活,但頻繁的修復(fù)會增加出錯幾率,導(dǎo)致這些區(qū)域更容易積累新的突變。
通訊作者、耶路撒冷希伯來大學(xué)的Rami Aqeilan教授稱:“癌細(xì)胞依靠超級增強子來維持生長基因的高速運轉(zhuǎn)?!?/div>
“我們發(fā)現(xiàn),這種高產(chǎn)出的活動會給DNA帶來巨大的壓力,形成DNA斷裂熱點,細(xì)胞必須反復(fù)修復(fù)這些斷裂。這種循環(huán)或許能在短期內(nèi)幫助腫瘤存活,但同時也增加了突變風(fēng)險,可能推動癌癥演化?!?/div>
圖1 超級增強子塑造癌癥中轉(zhuǎn)錄相關(guān)DNA斷裂的分布格局與修復(fù)動態(tài)
第一作者Osama Hidmi補充說:“令人興奮的是,由于癌細(xì)胞依賴這些高壓力DNA區(qū)域來維持生長,它們在此處也更容易受到攻擊。這為靶向腫瘤賴以生存的機制進(jìn)行治療打開了大門?!?/div>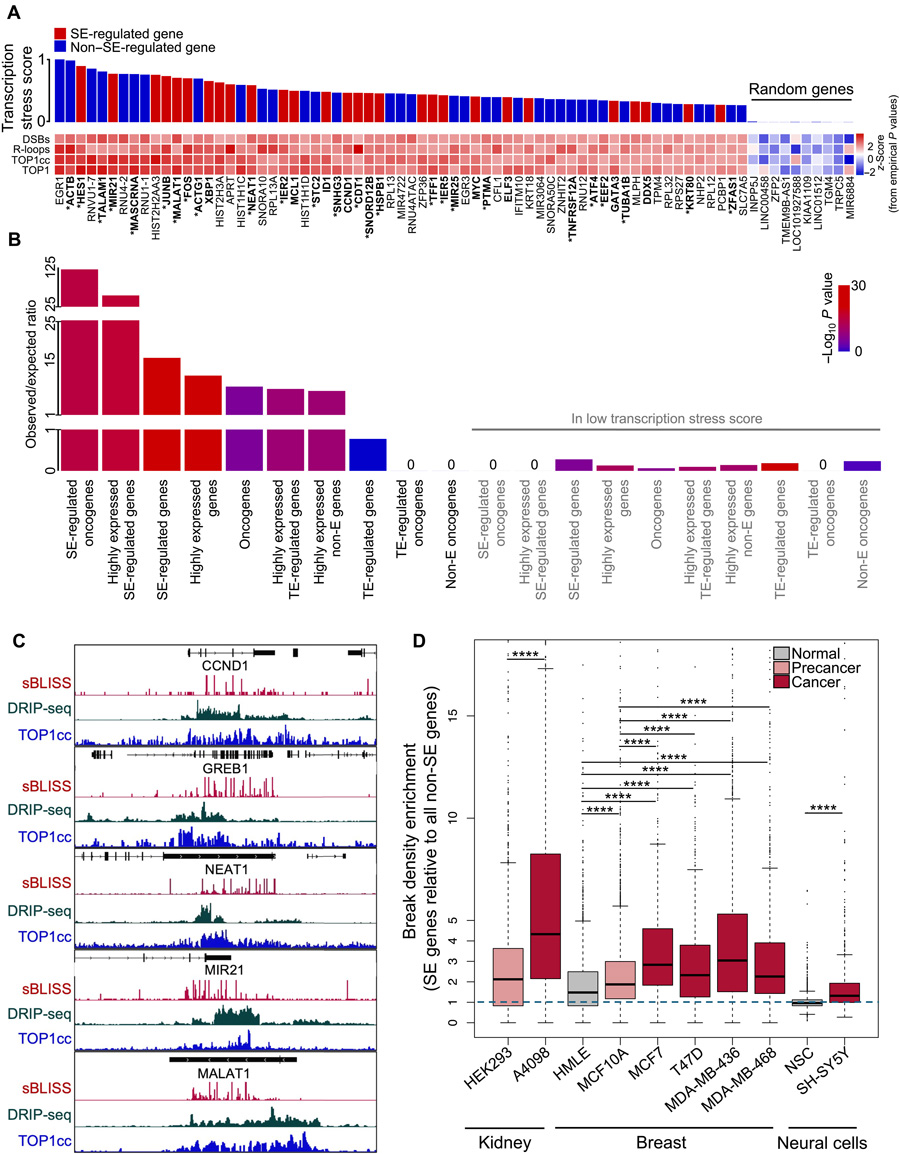
圖2 受超級增強子調(diào)控的致癌基因是主要的轉(zhuǎn)錄應(yīng)激位點

圖2 受超級增強子調(diào)控的致癌基因是主要的轉(zhuǎn)錄應(yīng)激位點
DNA損傷和修復(fù)是癌癥生長、變異和耐藥的核心機制。這項研究有助于解釋一些重要損傷發(fā)生的位置及其成因。
研究表明,癌癥中最強的基因調(diào)控區(qū)域也是DNA反復(fù)承受壓力的部位,這指出了腫瘤的潛在薄弱點,這些區(qū)域可能對抑制基因活性或干擾DNA修復(fù)的療法尤為敏感。了解這一過程有助于研究人員設(shè)計出阻止癌癥適應(yīng)和進(jìn)化的策略。
這項研究揭示了癌癥的生長驅(qū)動力如何破壞其自身DNA,有助于人們了解腫瘤為何具有侵襲性且遺傳上不穩(wěn)定。最終,科學(xué)界有望利用這種不穩(wěn)定性來對付癌癥。
參考資料
[1] Pharmacological Inhibition of EZH2 by GSK-343 Attenuates Neuroinflammation in a Mouse Model of Spinal Cord Injury
摘要:研究人員近日發(fā)現(xiàn),癌細(xì)胞中最強大的遺傳“開關(guān)”——超級增強子,會驅(qū)動異常高的基因活性。
耶路撒冷希伯來大學(xué)的研究人員近日發(fā)現(xiàn),癌細(xì)胞中最強大的遺傳“開關(guān)”——超級增強子,會驅(qū)動異常高的基因活性。這種高速運轉(zhuǎn)會給DNA帶來壓力,并可能導(dǎo)致危險的雙鏈斷裂。
癌細(xì)胞通常能夠修復(fù)這些損傷,但修復(fù)過程常常會出錯,反復(fù)的斷裂和修復(fù)會使這些區(qū)域更容易隨時間而積累突變。
簡單地說,幫助癌癥快速生長的機制也可能使DNA變得更加脆弱,這有助于解釋腫瘤如何持續(xù)演化,并在某些情況下變得更具侵襲性。
這項研究成果于1月21日發(fā)表在《Science Advances》雜志上。

圖1 超級增強子塑造癌癥中轉(zhuǎn)錄相關(guān)DNA斷裂的分布格局與修復(fù)動態(tài)
癌癥的特征是不受控制的增殖,并伴隨著致癌基因過度轉(zhuǎn)錄,這會引發(fā)轉(zhuǎn)錄應(yīng)激。這種應(yīng)激是導(dǎo)致DNA雙鏈斷裂的主要原因,進(jìn)而危及基因組穩(wěn)定性。
盡管轉(zhuǎn)錄應(yīng)激至關(guān)重要,但其整體景觀及后果仍未被充分探索。
研究人員將重點放在超級增強子上,這些片段能夠增強附近基因的活性,使驅(qū)動癌癥的基因程序保持高水平運行。
他們利用一種稱為sBLISS的基因組作圖方法,繪制出了雙鏈斷裂的詳細(xì)圖譜。雙鏈斷裂(DSB)是最嚴(yán)重的DNA損傷類型之一,其特征是DNA分子的兩條鏈同時斷裂。
這些斷裂并非隨機分布:它們聚集在由超級增強子驅(qū)動的基因內(nèi),這表明當(dāng)癌癥迫使某些基因持續(xù)表達(dá)時,可能會使系統(tǒng)承受過大的壓力,從而引發(fā)斷裂。
研究人員還追蹤了細(xì)胞用來標(biāo)記DNA損傷并調(diào)動修復(fù)機制的天然“警報”信號。他們發(fā)現(xiàn),這些高活性區(qū)域會反復(fù)發(fā)生DNA斷裂和修復(fù)。盡管這有助于腫瘤存活,但頻繁的修復(fù)會增加出錯幾率,導(dǎo)致這些區(qū)域更容易積累新的突變。
通訊作者、耶路撒冷希伯來大學(xué)的Rami Aqeilan教授稱:“癌細(xì)胞依靠超級增強子來維持生長基因的高速運轉(zhuǎn)。”
“我們發(fā)現(xiàn),這種高產(chǎn)出的活動會給DNA帶來巨大的壓力,形成DNA斷裂熱點,細(xì)胞必須反復(fù)修復(fù)這些斷裂。這種循環(huán)或許能在短期內(nèi)幫助腫瘤存活,但同時也增加了突變風(fēng)險,可能推動癌癥演化?!?/div>
圖2 受超級增強子調(diào)控的致癌基因是主要的轉(zhuǎn)錄應(yīng)激位點
第一作者Osama Hidmi補充說:“令人興奮的是,由于癌細(xì)胞依賴這些高壓力DNA區(qū)域來維持生長,它們在此處也更容易受到攻擊。這為靶向腫瘤賴以生存的機制進(jìn)行治療打開了大門。”

圖2 受超級增強子調(diào)控的致癌基因是主要的轉(zhuǎn)錄應(yīng)激位點
DNA損傷和修復(fù)是癌癥生長、變異和耐藥的核心機制。這項研究有助于解釋一些重要損傷發(fā)生的位置及其成因。
研究表明,癌癥中最強的基因調(diào)控區(qū)域也是DNA反復(fù)承受壓力的部位,這指出了腫瘤的潛在薄弱點,這些區(qū)域可能對抑制基因活性或干擾DNA修復(fù)的療法尤為敏感。了解這一過程有助于研究人員設(shè)計出阻止癌癥適應(yīng)和進(jìn)化的策略。
這項研究揭示了癌癥的生長驅(qū)動力如何破壞其自身DNA,有助于人們了解腫瘤為何具有侵襲性且遺傳上不穩(wěn)定。最終,科學(xué)界有望利用這種不穩(wěn)定性來對付癌癥。
參考資料
[1] Pharmacological Inhibition of EZH2 by GSK-343 Attenuates Neuroinflammation in a Mouse Model of Spinal Cord Injury



